溃疡性结肠炎
正确答案:
溃疡性结肠炎又称慢性非特异性溃疡性结肠炎,是一种病因不明的直肠和结肠的炎性疾病。病变局限在大肠黏膜与黏膜下层,且以溃疡为主。可发生在任何年龄,以青壮年多见,亦可见于儿童或老年,男稍多于女。欧美国家本病发病率较高,我国近年也有所增加。
【病因及发病机制】
溃疡性结肠炎病因和发病机制至今尚未完全明确,但多数认为与下列因素有关。
1.免疫因素 本病和免疫密切相关:①大多数患者伴发结节性红斑、虹膜炎、系统性红斑狼疮、自身免疫性溶血性贫血等免疫性疾病,且用肾上腺皮质激素治疗常能奏效。②患者血清中有抗自身结肠上皮细胞的抗体,并与大肠杆菌O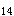 型有交叉免疫反应。③已用荧光免疫方法在动物中成功地制成了实验性溃疡性结肠炎模型。
型有交叉免疫反应。③已用荧光免疫方法在动物中成功地制成了实验性溃疡性结肠炎模型。
2.遗传因素 本病发病率在种族间有明显差异,白种人远高于黄种人和黑种人,10%~20%患者有家族史。
3.感染因素 溃疡性结肠炎可能由痢疾杆菌、溶组织阿米巴或病毒、真菌所引起,病原微生物乃至食物抗原可能是其非特异性促发因素。但至今未检出与本病有恒定明确关系的病原体。
4.精神神经因素 本病可因紧张、劳累而诱发,患者常有精神紧张和焦虑表现。由于大脑皮层活动障碍,可通过自主神经系统引起肠道运动亢进、肠血管平滑肌痉挛收缩、组织缺氧、毛细血管通透性增加,从而使结肠黏膜发生炎症、糜烂及溃疡。
溃疡性结肠炎的发病机制可概括为:遗传易感者通过环境、外源因素使肠黏膜损伤,致敏肠道淋巴组织,导致免疫调节和反馈失常,形成自身免疫反应而出现慢性、持续的炎症反应。参与此反应的细胞成分有巨噬细胞、肥大细胞、中性粒细胞、嗜酸细胞、T和B淋巴细胞及NK细胞;参与反应的细胞因子和炎性介质有γ干扰素、白细胞介素、肿瘤坏死因子、血小板激活因子、前列腺素样物质、白三烯、血栓素、组胺、5-羟色胺、神经多肽、血管活性肽、P物质、氧自由基等。
【临床表现】
起病缓慢,少数急性起病,偶见暴发。病程呈慢性过程,多表现为发作期与缓解期交替,少数症状持续并逐渐加重。精神刺激、劳累、饮食失调、继发感染为其诱因。
1.消化系统表现
(1)腹泻 腹泻为最主要的症状,常反复发作或持续不愈,轻者每天排便2~4次,可为软便、稀糊状,便血轻或无。重者排便频繁,可1~2小时1次,脓血显见,甚至大量便血。黏液血便是本病活动期的重要表现。病变局限在直肠者,鲜血附于粪便表面;病变扩展至直肠以上者,血液混于粪便中。病变累及直肠时,可有里急后重。
(2)腹痛 轻型患者在病变缓解期可无腹痛,或仅有腹部不适,部位多在左下或下腹部,亦可涉及全腹,有疼痛→便意→排便→缓解的规律。如果炎症波及腹膜,可见持续剧烈腹痛。
(3)其他症状 患者可有腹胀,严重病例有食欲不振、恶心、呕吐。
(4)体征 轻中型患者仅左下腹部压痛,有些患者可触及呈管状的乙状结肠。若有腹肌紧张、反跳痛、肠鸣音减弱,应警惕结肠扩张、肠穿孔等并发症。
2.全身症状 急性期可有发热,重症常出现高热,病情持续活动可出现衰弱、消瘦、贫血、低蛋白血症、电解质紊乱等表现。尤易发生低钾血症。
3.肠外表现本 病可伴有多种肠外表现,如关节炎、结节性红斑、虹膜炎、强直性脊柱炎、坏疽性脓皮病、口腔复发性溃疡、慢性肝炎等。
4.临床分型
(1)根据病情经过分型
1)初发型:首次发病。
2)慢性复发型:临床多见,本型病变范围小,症状轻,发作与缓解交替,预后好。
3)慢性持续型:症状持续半年以上,提示病变广泛。
4)急性感染型:少见。起病急骤,全身和消化系症状严重,常并发结肠扩张、肠穿孔、下消化道出血、败血症等。
(2)根据病情程度分型
1)轻型:腹泻每天4次以下,无发热,贫血和便血轻或无,血沉正常。
2)中型:介于轻、重型之间,腹泻每天4次以上,仅伴有轻微全身表现。
3)重型:腹泻每天6次以上,多为肉眼脓血便,体温>38℃至少持续2天以上,脉搏>100次/分,血红蛋白≤70g/L,血沉>30mm/h,血清白蛋白<30g/L,体重短期内明显减轻。常有严重的腹痛,腹泻,全腹压痛,严重者可出现失水和虚脱等毒血症征象。
(3)根据病变范围分型可分为直肠炎、直肠乙状结肠炎、左半结肠炎、广泛性或全结肠炎等。如果病变是区域性分布者,又称区域性结肠炎。
(4)根据病情分期可分为活动期和缓解期。
3.并发症
(1)结肠扩张 多见于暴发性溃疡性结肠炎和全结肠炎患者,因炎症侵及肌层,结肠失去收缩力造成结肠扩张。低钾、应用抗胆碱能药物、吗啡制剂及灌肠是诱发因素。临床表现为病情急剧变化,毒血症明显,有脱水与电解质紊乱,出现鼓肠,腹部压痛,肠鸣音减弱或消失,X线腹部平片可见结肠扩大、结肠袋消失。易引起急性肠穿孔,预后差。
(2)结肠大出血 溃疡累及血管可引起大出血。
(3)其他 可并发癌变、肠梗阻、瘘管及肛周脓肿等。病期长达10年以上,病变广泛,年龄在40岁以上者易恶变。
【实验室及其他检查】
1.血液检查
(1)血红蛋白降低,为小细胞低色素性贫血。急性期中性粒细胞增多。
(2)血沉增快。凝血酶原时间延长,血浆第Ⅲ、Ⅶ、Ⅷ因子的活性增加,血小板计数升高。
(3)严重者血清白蛋白降低。血清蛋白电泳示α 和α
和α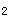 球蛋白明显升高。在缓解期α
球蛋白明显升高。在缓解期α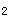 球蛋白增加,常为复发的信号。在发作时期γ球蛋白下降常提示预后不良。
球蛋白增加,常为复发的信号。在发作时期γ球蛋白下降常提示预后不良。
(4)C反应蛋白增高,IgG稍高。
(5)严重者出现电解质紊乱,尤以低钾最明显。
2.粪便检查 常有黏液脓血便,镜检见红细胞、白细胞和巨噬细胞。粪便培养致病菌阴性。
3.结肠镜检查 结肠镜检查具有诊断意义,可直接观察肠黏膜变化,准确了解病变范围。内镜下所见特征是:急性期肠黏膜充血水肿,分泌亢进,湿润,可有针尖大小的红色斑点和黄白色点状物,肠腔痉挛,皱襞减少。在慢性期,黏膜粗糙不平,呈细颗粒状,黏膜血管模糊,质脆易出血,有大小、形状、色泽多样的假息肉,有时呈拱桥状增生。活组织检查显示特异性炎性病变和纤维瘢痕,同时可见糜烂、隐窝脓肿、腺体排列异常及上皮变化等。
4.X线检查 应用X线气钡双重对比造影,有利于观察黏膜形态。X线征象主要有:①病变肠管痉挛,中心性狭窄;②病变肠管结肠袋变浅、消失,肠管边缘显示多数毛刺状突出的小龛影;③肠黏膜紊乱;④慢性期肠管呈持续性狭窄,边缘僵直,肠管缩短。
【诊断与鉴别诊断】
1.诊断 本病的主要诊断依据包括慢性腹泻、脓血黏液便、腹痛,不同程度全身症状,反复发作的趋势;多次粪检无病原体发现,内镜检查及X线钡剂灌肠显示结肠炎病变等。完整的诊断应包括临床类型、严重程度、病变范围及病情分期。
2.鉴别诊断
(1)细菌性痢疾 常有菌痢病史,粪便培养分离出痢疾杆菌,结肠镜检时取其脓性分泌物培养阳性率较高,抗菌药物治疗有效。
(2)慢性阿米巴痢疾 病变主要侵犯近端结肠,溃疡较深,其边缘为潜行性,溃疡间的黏膜多属正常,粪便检查或通过结肠镜取溃疡渗出物做镜检可找到溶组织阿米巴滋养体,抗阿米巴治疗有效。
(3)结肠癌 多见于中年以上,直肠指检可触及肿块,肠镜及钡剂灌肠检查对鉴别诊断有价值。
(4)血吸虫病
(5)肠易激综合征
(6)克罗恩病
此外,还应与其他感染性肠炎鉴别,如肠结核、沙门菌结肠炎、抗菌药物相关性肠炎、真菌性肠炎、缺血性肠炎、放射性肠炎、结肠息肉、结肠憩室炎、白塞病等。
【治疗】
主要采用内科治疗,其原则是控制急性发作,缓解病情,减少复发,防止并发症。
1.一般治疗 注意休息,劳逸结合,急性发作或重症患者应住院治疗,饮食宜少渣易消化,营养均衡,足够热量,少脂肪,避免生冷和刺激性食物,并给予支持疗法。及时纠正水、电解质平衡紊乱,贫血者可输血,低蛋白血症者输入血清蛋白。病情严重者应禁食,给予完全胃肠外营养治疗。腹痛患者可酌情用抗胆碱能药物,但不宜多用,否则促发急性结肠扩张。腹泻严重者可谨慎试用复方苯乙哌啶或洛哌丁胺等。
2.药物治疗
(1)氨基水杨酸制剂 常用柳氮磺吡啶,该药20%~30%自小肠吸收,不经代谢而从胆汁排出,75%在大肠经肠菌裂解为5-氨基水杨酸及磺胺吡啶。每天4g,分4次口服,用药3~4周病情缓解后改为每天2g,维持1~2年。不良反应有恶心、呕吐、皮疹、白细胞减少及溶血反应等,并干扰叶酸的吸收,导致贫血、精子数量减少及形态异常,停药3个月可恢复。服用柳氮磺吡啶的同时应补充叶酸1~2mg/d。近年已研制成5-ASA的特殊制剂,如奥沙拉嗪、巴柳氮,为缓释片或控释片,能到达远端回肠和结肠发挥药效,疗效与SASP相仿,但不良反应明显减少。如果病变局限在直肠,可用SASP或5-ASA灌肠,也可使用栓剂。
(2)糖皮质激素 基本作用为非特异性抗炎和抑制免疫反应。适用于重型或暴发型,或柳氮磺吡啶治疗无效的轻型、中型患者。一般用泼尼松每天30~40mg,分3~4次口服,病情控制后逐渐减量至每天10~15mg,维持半年左右停药。重型患者常用氢化可的松每天200~300mg静脉滴注,1周后改为口服泼尼松60mg/d,病情控制后,逐渐减量至停药。皮质激素亦可用于灌肠,每次用琥珀酸氢化可的松50~100mg保留灌肠,每天1~2次,病情好转后改为每周2~3次,疗程1~3周。
(3)免疫抑制剂 上述两类药物治疗无效者可试用硫唑嘌呤,每天每千克体重1.5mg,分2~3次口服;近年来应用甲氨蝶呤、环孢素,有时获得良好疗效。青霉胺、干扰素等也有一定疗效。
3.手术治疗 当出现癌变、肠穿孔或濒临穿孔、脓肿或瘘管形成、大量或反复严重出血、结肠扩张等并发症,以及长期内科治疗无效者,应考虑外科手术治疗。
【病因及发病机制】
溃疡性结肠炎病因和发病机制至今尚未完全明确,但多数认为与下列因素有关。
1.免疫因素 本病和免疫密切相关:①大多数患者伴发结节性红斑、虹膜炎、系统性红斑狼疮、自身免疫性溶血性贫血等免疫性疾病,且用肾上腺皮质激素治疗常能奏效。②患者血清中有抗自身结肠上皮细胞的抗体,并与大肠杆菌O
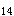 型有交叉免疫反应。③已用荧光免疫方法在动物中成功地制成了实验性溃疡性结肠炎模型。
型有交叉免疫反应。③已用荧光免疫方法在动物中成功地制成了实验性溃疡性结肠炎模型。2.遗传因素 本病发病率在种族间有明显差异,白种人远高于黄种人和黑种人,10%~20%患者有家族史。
3.感染因素 溃疡性结肠炎可能由痢疾杆菌、溶组织阿米巴或病毒、真菌所引起,病原微生物乃至食物抗原可能是其非特异性促发因素。但至今未检出与本病有恒定明确关系的病原体。
4.精神神经因素 本病可因紧张、劳累而诱发,患者常有精神紧张和焦虑表现。由于大脑皮层活动障碍,可通过自主神经系统引起肠道运动亢进、肠血管平滑肌痉挛收缩、组织缺氧、毛细血管通透性增加,从而使结肠黏膜发生炎症、糜烂及溃疡。
溃疡性结肠炎的发病机制可概括为:遗传易感者通过环境、外源因素使肠黏膜损伤,致敏肠道淋巴组织,导致免疫调节和反馈失常,形成自身免疫反应而出现慢性、持续的炎症反应。参与此反应的细胞成分有巨噬细胞、肥大细胞、中性粒细胞、嗜酸细胞、T和B淋巴细胞及NK细胞;参与反应的细胞因子和炎性介质有γ干扰素、白细胞介素、肿瘤坏死因子、血小板激活因子、前列腺素样物质、白三烯、血栓素、组胺、5-羟色胺、神经多肽、血管活性肽、P物质、氧自由基等。
【临床表现】
起病缓慢,少数急性起病,偶见暴发。病程呈慢性过程,多表现为发作期与缓解期交替,少数症状持续并逐渐加重。精神刺激、劳累、饮食失调、继发感染为其诱因。
1.消化系统表现
(1)腹泻 腹泻为最主要的症状,常反复发作或持续不愈,轻者每天排便2~4次,可为软便、稀糊状,便血轻或无。重者排便频繁,可1~2小时1次,脓血显见,甚至大量便血。黏液血便是本病活动期的重要表现。病变局限在直肠者,鲜血附于粪便表面;病变扩展至直肠以上者,血液混于粪便中。病变累及直肠时,可有里急后重。
(2)腹痛 轻型患者在病变缓解期可无腹痛,或仅有腹部不适,部位多在左下或下腹部,亦可涉及全腹,有疼痛→便意→排便→缓解的规律。如果炎症波及腹膜,可见持续剧烈腹痛。
(3)其他症状 患者可有腹胀,严重病例有食欲不振、恶心、呕吐。
(4)体征 轻中型患者仅左下腹部压痛,有些患者可触及呈管状的乙状结肠。若有腹肌紧张、反跳痛、肠鸣音减弱,应警惕结肠扩张、肠穿孔等并发症。
2.全身症状 急性期可有发热,重症常出现高热,病情持续活动可出现衰弱、消瘦、贫血、低蛋白血症、电解质紊乱等表现。尤易发生低钾血症。
3.肠外表现本 病可伴有多种肠外表现,如关节炎、结节性红斑、虹膜炎、强直性脊柱炎、坏疽性脓皮病、口腔复发性溃疡、慢性肝炎等。
4.临床分型
(1)根据病情经过分型
1)初发型:首次发病。
2)慢性复发型:临床多见,本型病变范围小,症状轻,发作与缓解交替,预后好。
3)慢性持续型:症状持续半年以上,提示病变广泛。
4)急性感染型:少见。起病急骤,全身和消化系症状严重,常并发结肠扩张、肠穿孔、下消化道出血、败血症等。
(2)根据病情程度分型
1)轻型:腹泻每天4次以下,无发热,贫血和便血轻或无,血沉正常。
2)中型:介于轻、重型之间,腹泻每天4次以上,仅伴有轻微全身表现。
3)重型:腹泻每天6次以上,多为肉眼脓血便,体温>38℃至少持续2天以上,脉搏>100次/分,血红蛋白≤70g/L,血沉>30mm/h,血清白蛋白<30g/L,体重短期内明显减轻。常有严重的腹痛,腹泻,全腹压痛,严重者可出现失水和虚脱等毒血症征象。
(3)根据病变范围分型可分为直肠炎、直肠乙状结肠炎、左半结肠炎、广泛性或全结肠炎等。如果病变是区域性分布者,又称区域性结肠炎。
(4)根据病情分期可分为活动期和缓解期。
3.并发症
(1)结肠扩张 多见于暴发性溃疡性结肠炎和全结肠炎患者,因炎症侵及肌层,结肠失去收缩力造成结肠扩张。低钾、应用抗胆碱能药物、吗啡制剂及灌肠是诱发因素。临床表现为病情急剧变化,毒血症明显,有脱水与电解质紊乱,出现鼓肠,腹部压痛,肠鸣音减弱或消失,X线腹部平片可见结肠扩大、结肠袋消失。易引起急性肠穿孔,预后差。
(2)结肠大出血 溃疡累及血管可引起大出血。
(3)其他 可并发癌变、肠梗阻、瘘管及肛周脓肿等。病期长达10年以上,病变广泛,年龄在40岁以上者易恶变。
【实验室及其他检查】
1.血液检查
(1)血红蛋白降低,为小细胞低色素性贫血。急性期中性粒细胞增多。
(2)血沉增快。凝血酶原时间延长,血浆第Ⅲ、Ⅶ、Ⅷ因子的活性增加,血小板计数升高。
(3)严重者血清白蛋白降低。血清蛋白电泳示α
 和α
和α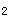 球蛋白明显升高。在缓解期α
球蛋白明显升高。在缓解期α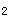 球蛋白增加,常为复发的信号。在发作时期γ球蛋白下降常提示预后不良。
球蛋白增加,常为复发的信号。在发作时期γ球蛋白下降常提示预后不良。(4)C反应蛋白增高,IgG稍高。
(5)严重者出现电解质紊乱,尤以低钾最明显。
2.粪便检查 常有黏液脓血便,镜检见红细胞、白细胞和巨噬细胞。粪便培养致病菌阴性。
3.结肠镜检查 结肠镜检查具有诊断意义,可直接观察肠黏膜变化,准确了解病变范围。内镜下所见特征是:急性期肠黏膜充血水肿,分泌亢进,湿润,可有针尖大小的红色斑点和黄白色点状物,肠腔痉挛,皱襞减少。在慢性期,黏膜粗糙不平,呈细颗粒状,黏膜血管模糊,质脆易出血,有大小、形状、色泽多样的假息肉,有时呈拱桥状增生。活组织检查显示特异性炎性病变和纤维瘢痕,同时可见糜烂、隐窝脓肿、腺体排列异常及上皮变化等。
4.X线检查 应用X线气钡双重对比造影,有利于观察黏膜形态。X线征象主要有:①病变肠管痉挛,中心性狭窄;②病变肠管结肠袋变浅、消失,肠管边缘显示多数毛刺状突出的小龛影;③肠黏膜紊乱;④慢性期肠管呈持续性狭窄,边缘僵直,肠管缩短。
【诊断与鉴别诊断】
1.诊断 本病的主要诊断依据包括慢性腹泻、脓血黏液便、腹痛,不同程度全身症状,反复发作的趋势;多次粪检无病原体发现,内镜检查及X线钡剂灌肠显示结肠炎病变等。完整的诊断应包括临床类型、严重程度、病变范围及病情分期。
2.鉴别诊断
(1)细菌性痢疾 常有菌痢病史,粪便培养分离出痢疾杆菌,结肠镜检时取其脓性分泌物培养阳性率较高,抗菌药物治疗有效。
(2)慢性阿米巴痢疾 病变主要侵犯近端结肠,溃疡较深,其边缘为潜行性,溃疡间的黏膜多属正常,粪便检查或通过结肠镜取溃疡渗出物做镜检可找到溶组织阿米巴滋养体,抗阿米巴治疗有效。
(3)结肠癌 多见于中年以上,直肠指检可触及肿块,肠镜及钡剂灌肠检查对鉴别诊断有价值。
(4)血吸虫病
(5)肠易激综合征
(6)克罗恩病
此外,还应与其他感染性肠炎鉴别,如肠结核、沙门菌结肠炎、抗菌药物相关性肠炎、真菌性肠炎、缺血性肠炎、放射性肠炎、结肠息肉、结肠憩室炎、白塞病等。
【治疗】
主要采用内科治疗,其原则是控制急性发作,缓解病情,减少复发,防止并发症。
1.一般治疗 注意休息,劳逸结合,急性发作或重症患者应住院治疗,饮食宜少渣易消化,营养均衡,足够热量,少脂肪,避免生冷和刺激性食物,并给予支持疗法。及时纠正水、电解质平衡紊乱,贫血者可输血,低蛋白血症者输入血清蛋白。病情严重者应禁食,给予完全胃肠外营养治疗。腹痛患者可酌情用抗胆碱能药物,但不宜多用,否则促发急性结肠扩张。腹泻严重者可谨慎试用复方苯乙哌啶或洛哌丁胺等。
2.药物治疗
(1)氨基水杨酸制剂 常用柳氮磺吡啶,该药20%~30%自小肠吸收,不经代谢而从胆汁排出,75%在大肠经肠菌裂解为5-氨基水杨酸及磺胺吡啶。每天4g,分4次口服,用药3~4周病情缓解后改为每天2g,维持1~2年。不良反应有恶心、呕吐、皮疹、白细胞减少及溶血反应等,并干扰叶酸的吸收,导致贫血、精子数量减少及形态异常,停药3个月可恢复。服用柳氮磺吡啶的同时应补充叶酸1~2mg/d。近年已研制成5-ASA的特殊制剂,如奥沙拉嗪、巴柳氮,为缓释片或控释片,能到达远端回肠和结肠发挥药效,疗效与SASP相仿,但不良反应明显减少。如果病变局限在直肠,可用SASP或5-ASA灌肠,也可使用栓剂。
(2)糖皮质激素 基本作用为非特异性抗炎和抑制免疫反应。适用于重型或暴发型,或柳氮磺吡啶治疗无效的轻型、中型患者。一般用泼尼松每天30~40mg,分3~4次口服,病情控制后逐渐减量至每天10~15mg,维持半年左右停药。重型患者常用氢化可的松每天200~300mg静脉滴注,1周后改为口服泼尼松60mg/d,病情控制后,逐渐减量至停药。皮质激素亦可用于灌肠,每次用琥珀酸氢化可的松50~100mg保留灌肠,每天1~2次,病情好转后改为每周2~3次,疗程1~3周。
(3)免疫抑制剂 上述两类药物治疗无效者可试用硫唑嘌呤,每天每千克体重1.5mg,分2~3次口服;近年来应用甲氨蝶呤、环孢素,有时获得良好疗效。青霉胺、干扰素等也有一定疗效。
3.手术治疗 当出现癌变、肠穿孔或濒临穿孔、脓肿或瘘管形成、大量或反复严重出血、结肠扩张等并发症,以及长期内科治疗无效者,应考虑外科手术治疗。
第十章 常见西医疾病